叶酸靶向荧光脂质体(FITC标记)是西安齐岳生物针对生物医药科研、临床前研究及相关产业化需求开发的功能性纳米载体,以脂质体为核心骨架,表面修饰叶酸配体实现靶向识别,通过FITC(荧光素)标记实现可视化追踪,兼具靶向递送、荧光示踪、生物相容性优良等核心优势,广泛应用于肿瘤细胞成像、药物递送追踪、细胞分子定位等领域,可根据客户具体需求提供全维度定制服务,助力科研与产业转化。

一、定制内容
西安齐岳生物依托成熟的磷脂修饰、及靶向偶联技术平台,针对叶酸靶向荧光脂质体(FITC标记)提供多维度定制服务,精准匹配不同实验场景与需求,细分方向如下:
(一)脂质体核心参数定制
• 粒径定制:可定制50-200nm范围内不同粒径规格,默认100-150nm(适配细胞摄取与体内循环),可通过挤出法、微流控法精准调控粒径均一性,确保PDI<0.2。
• 纯度与稳定性定制:磷脂纯度≥95%,FITC标记效率≥85%,叶酸修饰率≥90%,可定制常温/冷藏稳定型产品,添加*氧化剂或稳定剂延长保存周期,避免荧光淬灭与脂质体破裂。
• 剂型定制:提供混悬液(PBS缓冲液)、冻干粉两种剂型,冻干粉可定制真空包装,复溶后稳定性良好,适配长期储存与运输需求。
(二)功能化定制
• 靶向增强定制:可增加PEG化修饰(如DSPE-PEG2000),构建长循环体系,减少网状内皮系统吞噬,延长体内循环时间;可调节叶酸修饰密度,适配不同叶酸受体表达水平的细胞/组织研究。
• 荧光性能定制:优化FITC标记方式(无铜点击化学、EDC/NHS酰胺键偶联等),提升荧光稳定性,降低荧光淬灭率(淬灭率<3%);可搭配双(如FITC+Cy5),实现多通道成像与追踪。
• 载药定制:可定制载药型叶酸靶向荧光脂质体,适配疏水/亲水小分子药物、核酸(siRNA、mRNA)、蛋白/多肽等,优化包封工艺,确保包封率≥80%(小分子药物)、≥90%(核酸),实现靶向递药与荧光示踪同步进行。
• 响应性定制:可引入pH敏感(腙键)、还原敏感(二硫键)连接臂,实现肿瘤微环境(pH<6.5、高GSH浓度)下的荧光信号增强或药物智能释放,适配靶向*与成像一体化研究。
(三)规格与实验适配定制
• 科研级规格:1mg、5mg、10mg、50mg/瓶,可按需定制小试量(毫克级)或中试量(克级),适配细胞实验、动物实验等不同阶段需求。
• 实验场景适配:针对细胞表面分子成像、活体肿瘤示踪、药物递送动力学研究等不同场景,定制适配的脂质体分散性、表面电荷(Zeta电位),确保实验重复性与数据准确性,提供专属实验方案指导。
二、具体产品
产品名称 | 规格 | 适用场景 |
叶酸靶向FITC标记脂质体(标准型) | 10mg/瓶、50mg/瓶 | 常规细胞成像、肿瘤细胞靶向识别实验 |
PEG化叶酸靶向FITC脂质体 | 5mg/瓶、20mg/瓶 | 体内活体示踪、长期药物递送追踪 |
载药型叶酸靶向FITC脂质体 | 定制规格(1-50mg) | 靶向药物递送、药效学与成像一体化研究 |
双叶酸靶向脂质体(FITC+Cy5) | 定制规格(1-10mg) | 细胞内定位、脂质体摄取动力学研究 |
三、案例分享
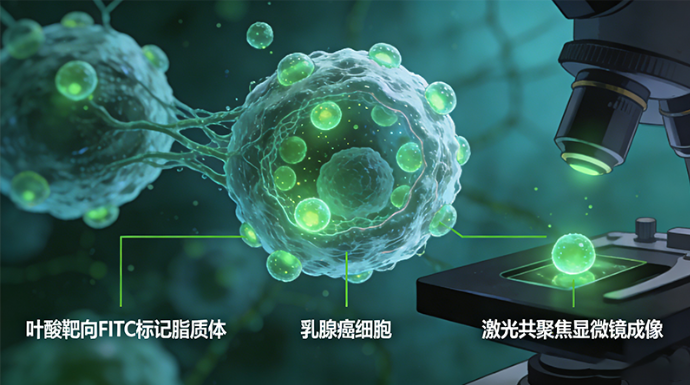
案例1:某高校肿瘤生物学课题组定制需求
客户需求:定制叶酸靶向FITC标记脂质体,规格20mg,粒径100-120nm,适配乳腺癌细胞(高表达叶酸受体)成像,要求荧光稳定性强,无明显淬灭,可用于激光共聚焦显微镜观察,提供完整表征数据。
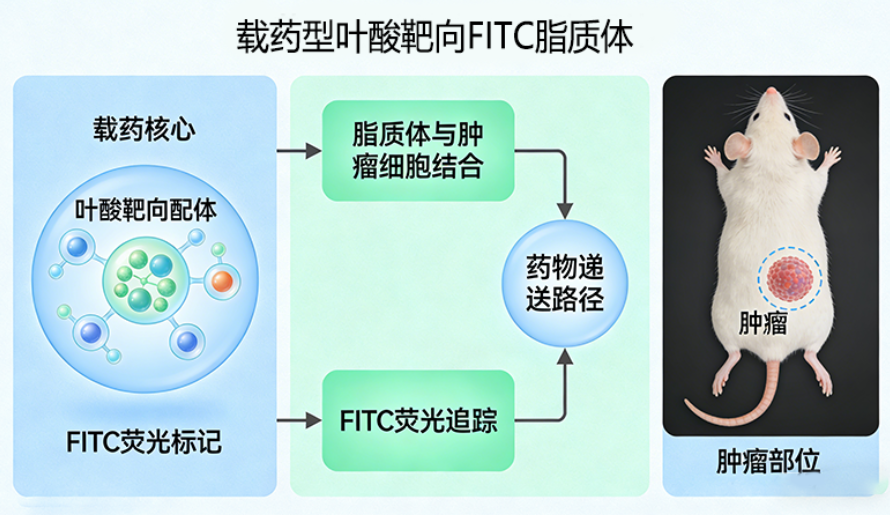
案例2:某药企临床前研发定制需求
客户需求:定制载药型叶酸靶向FITC脂质体,负载疏水化疗药物,规格50mg,包封率≥85%,叶酸修饰率≥90%,适配小鼠肿瘤模型,实现药物递送追踪与靶向*同步,符合生物医药行业质控标准。
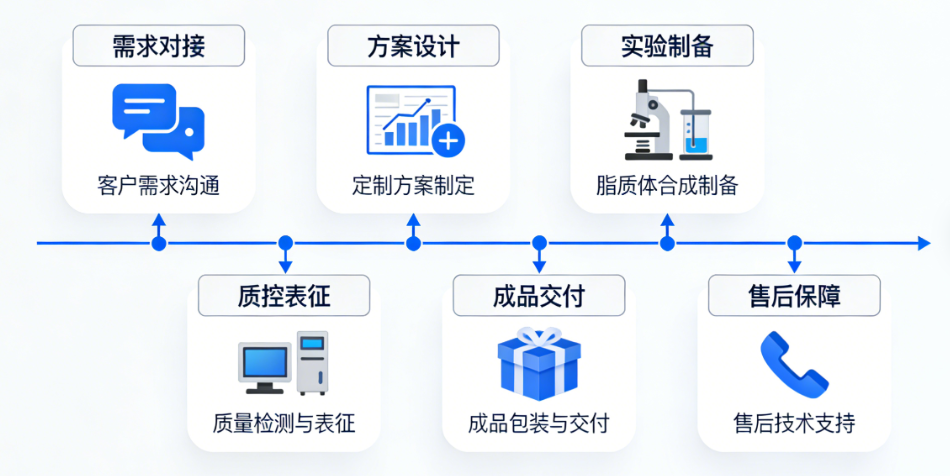
四、服务流程
1. 需求对接:一对一技术沟通,明确定制参数、规格、实验场景及交付要求;
2. 方案设计:结合需求制定个性化制备方案,确认工艺、质控标准及交付周期;
3. 实验制备:按方案完成脂质体制备、FITC标记、叶酸修饰及纯化;
4. 质控表征:完成粒径、纯度、标记效率、稳定性等指标检测,出具检测报告;
5. 成品交付:按客户要求包装,同步提供使用说明、表征报告及技术支持;
6. 售后保障:提供实验指导,解决使用过程中的技术问题,支持后续定制优化。
五、参考文献
1. Allen, T. M., Cullis, P. R. Liposomal drug delivery systems: from concept to clinical applications. Advanced Drug Delivery Reviews, 2013, 65(1): 36-48.(脂质体递送系统经典综述,明确磷脂材料核心地位及靶向修饰优化方向)
2. Immordino ML, Dosio F, Cattel L. Pegylation of liposomes for anticancer drug delivery. International Journal of Pharmaceutics, 2006, 316(1-2): 1-20.(系统阐述磷脂PEG化改性机制及肿瘤药物递送应用)
3. Li Y, Zhang Y, Wang H, et al. pH-responsive phospholipid-PEG conjugates for targeted intracellular drug release in tumor microenvironment. Journal of Controlled Release, 2023, 358: 456-468.(刺激响应型磷脂改性与靶向递送研究)
4. Wang X, Zhao J, Chen L, et al. Development and application of phospholipid-PEG-biomacromolecule conjugates for gene delivery. Biomaterials Science, 2025, 13(7): 2012-2028.(磷脂与生物大分子偶联及基因递送应用)
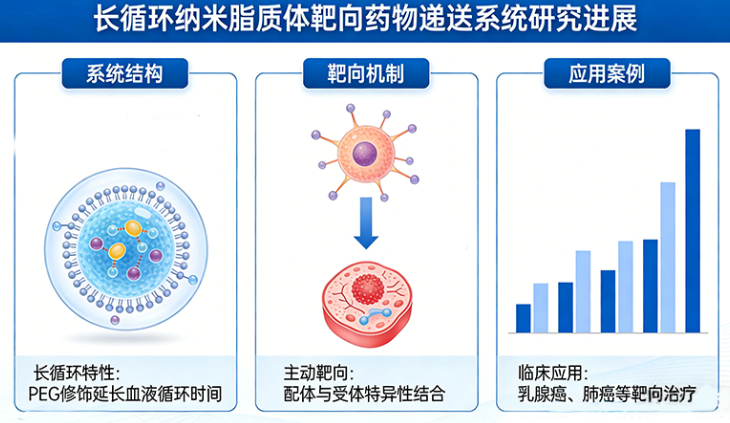
5. 苗数, 郭振超, 杨新明, 等. 长循环纳米脂质体靶向药物递送系统的研究进展. 纳米技术, 2025, 15(4): 109-117.(国内前沿磷脂改性与靶向偶联研究综述)
6. 刘杰, 张静, 李丽. 功能性磷脂材料的改性策略及在生物医学中的应用. 中国医药工业杂志, 2024, 55(3): 389-398.(国内医药工业领域磷脂改性技术规范文献)
7. Osinski, V., et al. In vivo liposomal delivery of PPARα/γ dual agonist tesaglitazar in a model of obesity enriches macrophage targeting and limits liver and kidney drug effects. Theranostics, 2020, 10(2): 789-802.(脂质体体内靶向递送与示踪研究)
8. Zhang, Q., Li, Y., & Wang, L. (2023). N-terminal dual protein functionalization by strain-promoted alkyne–nitrone cycloaddition. Organic Letters, 25(18), 3321-3325.(无铜点击化学在生物分子偶联中的应用,支撑FITC标记工艺)
西安齐岳生物深耕功能性脂质体研发与定制领域,依托成熟的技术平台、严格的质控体系及专业的技术团队,为客户提供从产品定制、实验指导到售后保障的一站式服务,助力科研成果转化与产业化推进。




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询